
오랜 시간 사용해도 한 번도 고장 나지 않은 휴대폰, 마치 공연장에 있는 듯한 생생한 음질을 자랑하는 스피커. 일상생활에서 기대 이상으로 뛰어난 성능의 제품을 만나면 ‘품질이 좋다’고 감탄하는 순간이 있습니다.
소비재에서는 좋은 품질이 탁월한 제품력을 의미한다면, 바이오의약품 세계에서 좋은 품질이란 더 넓은 범위를 뜻합니다. 사람의 건강과 생명에 직접적인 영향력을 미치기 때문에 탁월한 제품력(=의약품의 효능과 안전성) 보장은 기본이고, 개발부터 생산, 유통, 사용에 이르는 전 과정에서 규제기관의 엄격한 품질 기준을 지키고 있음을 확인받았다는 뜻입니다.
바이오 업계의 헌법, ‘GMP’
바이오의약품은 최종 사용자인 환자의 생명과 맞닿아 있기에 GMP(Good Manufacturing and Practice)라는 엄격한 의약품 제조와 품질 관리 기준 아래 만들어집니다. GMP는 1900년대 초 미국에서 인체에 유해한 성분을 의약품 라벨에 표시하도록 규제한 것을 시작으로 오늘날에 이르기까지 그 개념이 강화되고 있습니다.
당시 육류 가공 산업의 비위생적인 환경을 폭로하는 내용을 담은 싱클레어의 소설 <정글(The Jungle)>이 미국 대중에게 큰 충격을 안기면서 식품, 의약품 안전에 관심을 불러일으켰고, 대중의 큰 관심은 미국 의회가 1906년 ‘식품 의약 조례(Pure Food and Drug Act)’를 통과시키며 미국 FDA 설립에 여파를 미쳤다고 알려져 있습니다. 이후 FDA는 식품 의약품 관련 기준을 발전시키며 1963년 세계 최초의 GMP 기준을 제정하게 되고, GMP는 바이오 업계의 헌법으로 자리 잡으며 점진적으로 진화해 왔습니다.
완벽한 품질의 시작은 ‘체계적인 시스템’
글로벌 제약사들은 GMP 규정 준수는 기본이고, 의약품 개발 단계부터 품질을 고려해 설계하는 접근법인 QbD(Quality by design)를 도입하는 등 품질 관리 체계를 강화하기 위해 자체 품질 관리 프로그램을 개발하고 인증을 획득하기도 합니다.
삼성바이오로직스는 글로벌 제약사와 규제 기관의 엄격한 조건을 충족하는 체계적인 품질 시스템을 갖추고 품질 마인드셋과 품질 문화를 더욱 강화해 나가고 있습니다. 중앙화/일원화된 품질 조직이 전체 공장의 품질을 책임지는 한편, 품질 시스템의 디지털화를 통해 능동적인 품질 활동을 진행하는 중입니다.
여은아 그룹장(Client Quality 3 그룹)은 “삼성바이오로직스는 약 100여개 이상의 제약사와 프로젝트를 함께해오며 거의 매주 고객사 및 규제기관과 실사를 진행하고 있는데, 이는 품질 시스템과 품질 문화에 대한 피드백을 얻을 수 있는 기회”라며, “지속적으로 품질 피드백을 받고, 개선하는 부분은 삼성바이오로직스의 품질 시스템을 더욱 견고하게 만드는 핵심 요소 중 하나”라고 설명했습니다.

매주 고객사와의 실사가 이뤄지는 삼성바이오로직스의 생산 현장
삼성바이오로직스는 CDMO 업계 최초로 기업 통합 품질 관리 시스템 EQUIS를 도입해 고객사가 시간과 장소에 상관없이 공정 관련 기록 확인과 프로젝트 문서의 열람과 승인을 가능하게 함으로써 협업 속도와 데이터의 투명성을 높이고 있으며, 디지털화에 따른 정보보호 관리 시스템도 강화하며 업계에서 유일하게 최고 권위의 국제 표준인 ISO 27001, ISO 27017을 모두 획득했습니다. 디지털 경쟁력과 철저한 보안을 기반으로 인공지능(AI) 등 더 진보한 기술을 품질 시스템에 적용하고 있습니다.
최현진 그룹장(Client Quality 2 그룹)은 “수십만 건의 품질 사례를 데이터베이스로 구축한 자체 개발 AI 플랫폼을 통해 과거 문서를 참조하여 표준작업절차서(Standard operating procedure)를 생성하고, 작업자가 신속하게 공정에 반영할 수 있도록 교육하고 있다”고 밝히며, AI 플랫폼과 함께 GMP 교육을 기반으로 한 삼성바이오로직스의 품질 교육 시간은 연간 21만 시간에 달한다고 전했습니다.
마침표 없는 세계
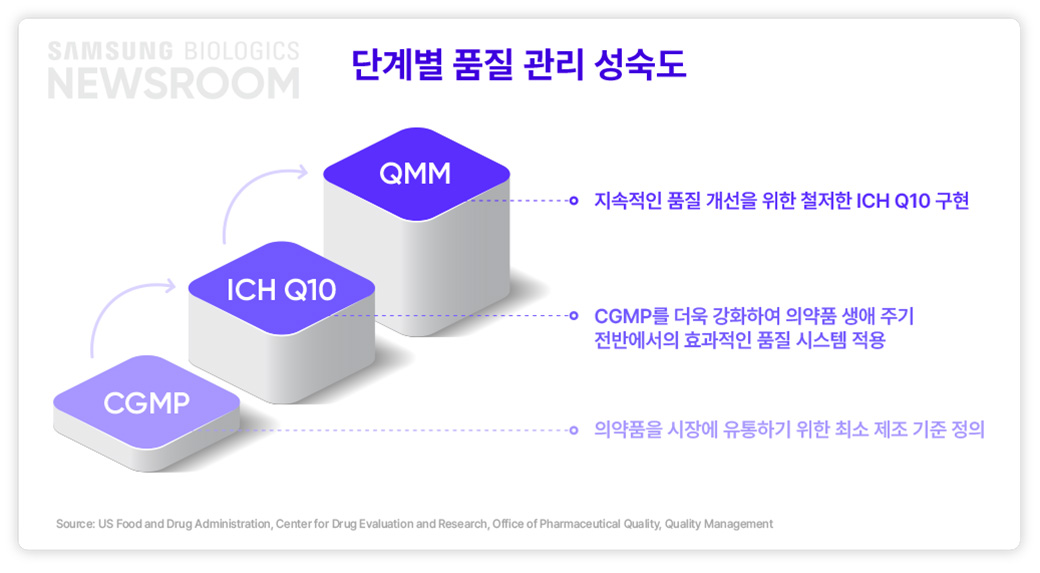
FDA는 지난 2022년, 의약품 부족의 60% 이상이 품질 이슈에서 발생한다고 언급하며, 단순한 규정 준수를 넘어 지속적인 의약품의 품질 개선을 이루고 강력한 품질 마인드 셋을 조성하기 위해 새로운 규제 관행으로 품질 관리 성숙도(QMM, Quality management maturity) 도입을 발표했습니다. ICH 또한 ICH Q10 모델*을 기반으로 전통적인 의약품 품질 개념에서 나아가 품질을 향하는 문화적 우수성과 운영 우수성을 포함하는 가이드라인을 제시하고 있습니다.
* 국제 의약품 규제 조화 위원회(ICH)가 개발한 의약품 산업을 위한 포괄적인 품질 관리 시스템 모델
품질 최우선 문화가 자연스럽게 스며들 수 있도록 삼성바이오로직스는 공정 중 일탈(deviation)이나 작업자의 오류(human error) 발생 시 자발적으로 공유하는 체계를 갖추고 있습니다. 품질 최우선 마인드와 견고한 시스템은 삼성바이오로직스가 글로벌 상위 제약사 20곳 중 17곳을 고객사로 확보할 수 있던 이유이기도 합니다.
정형석 팀장(Quality System&Compliance 팀)은 “삼성바이오로직스만의 품질 문화의 배경에는 함께 프로젝트를 수행하는 수많은 제약사들의 품질 시스템과 품질 마인드 셋을 경험하고 비교할 수 있는 글로벌 CDMO라는 특별한 위치가 있었다”고 설명하며, 품질은 우리 모두의 책임이고, 삼성바이오로직스의 존재 이유는 절대 타협할 수 없는 가치인 ‘품질’에 있다고 덧붙였습니다.
GMP 규정은 앞 글자에 대문자 C(Current)를 추가해 CGMP라는 이름으로도 불리는데, 이는 GMP규정이 고정 불변하는 것이 아니라 시대가 요구하는 수준에 맞게 적용되며 스스로 진화한다는 뜻을 내포합니다. 바이오의약품 품질의 세계에 마침표는 없기에, 삼성바이오로직스 역시 고품질의 바이오의약품을 환자에게 전달한다는 목표로 마침표 없는 품질을 향해 전진합니다.

오랜 시간 사용해도 한 번도 고장 나지 않은 휴대폰, 마치 공연장에 있는 듯한 생생한 음질을 자랑하는 스피커. 일상생활에서 기대 이상으로 뛰어난 성능의 제품을 만나면 ‘품질이 좋다’고 감탄하는 순간이 있습니다.
소비재에서는 좋은 품질이 탁월한 제품력을 의미한다면, 바이오의약품 세계에서 좋은 품질이란 더 넓은 범위를 뜻합니다. 사람의 건강과 생명에 직접적인 영향력을 미치기 때문에 탁월한 제품력(=의약품의 효능과 안전성) 보장은 기본이고, 개발부터 생산, 유통, 사용에 이르는 전 과정에서 규제기관의 엄격한 품질 기준을 지키고 있음을 확인받았다는 뜻입니다.
바이오 업계의 헌법, ‘GMP’
바이오의약품은 최종 사용자인 환자의 생명과 맞닿아 있기에 GMP(Good Manufacturing and Practice)라는 엄격한 의약품 제조와 품질 관리 기준 아래 만들어집니다. GMP는 1900년대 초 미국에서 인체에 유해한 성분을 의약품 라벨에 표시하도록 규제한 것을 시작으로 오늘날에 이르기까지 그 개념이 강화되고 있습니다.
당시 육류 가공 산업의 비위생적인 환경을 폭로하는 내용을 담은 싱클레어의 소설 <정글(The Jungle)>이 미국 대중에게 큰 충격을 안기면서 식품, 의약품 안전에 관심을 불러일으켰고, 대중의 큰 관심은 미국 의회가 1906년 ‘식품 의약 조례(Pure Food and Drug Act)’를 통과시키며 미국 FDA 설립에 여파를 미쳤다고 알려져 있습니다. 이후 FDA는 식품 의약품 관련 기준을 발전시키며 1963년 세계 최초의 GMP 기준을 제정하게 되고, GMP는 바이오 업계의 헌법으로 자리 잡으며 점진적으로 진화해 왔습니다.
완벽한 품질의 시작은
‘체계적인 시스템’
글로벌 제약사들은 GMP 규정 준수는 기본이고, 의약품 개발 단계부터 품질을 고려해 설계하는 접근법인 QbD(Quality by design)를 도입하는 등 품질 관리 체계를 강화하기 위해 자체 품질 관리 프로그램을 개발하고 인증을 획득하기도 합니다.
삼성바이오로직스는 글로벌 제약사와 규제 기관의 엄격한 조건을 충족하는 체계적인 품질 시스템을 갖추고 품질 마인드셋과 품질 문화를 더욱 강화해 나가고 있습니다. 중앙화/일원화된 품질 조직이 전체 공장의 품질을 책임지는 한편, 품질 시스템의 디지털화를 통해 능동적인 품질 활동을 진행하는 중입니다.
여은아 그룹장(Client Quality 3 그룹)은 “삼성바이오로직스는 약 100여개 이상의 제약사와 프로젝트를 함께해오며 거의 매주 고객사 및 규제기관과 실사를 진행하고 있는데, 이는 품질 시스템과 품질 문화에 대한 피드백을 얻을 수 있는 기회”라며, “지속적으로 품질 피드백을 받고, 개선하는 부분은 삼성바이오로직스의 품질 시스템을 더욱 견고하게 만드는 핵심 요소 중 하나”라고 설명했습니다.

매주 고객사와의 실사가 이뤄지는
삼성바이오로직스의 생산 현장
삼성바이오로직스는 CDMO 업계 최초로 기업 통합 품질 관리 시스템 EQUIS를 도입해 고객사가 시간과 장소에 상관없이 공정 관련 기록 확인과 프로젝트 문서의 열람과 승인을 가능하게 함으로써 협업 속도와 데이터의 투명성을 높이고 있으며, 디지털화에 따른 정보보호 관리 시스템도 강화하며 업계에서 유일하게 최고 권위의 국제 표준인 ISO 27001, ISO 27017을 모두 획득했습니다. 디지털 경쟁력과 철저한 보안을 기반으로 인공지능(AI) 등 더 진보한 기술을 품질 시스템에 적용하고 있습니다.
최현진 그룹장(Client Quality 2 그룹)은 “수십만 건의 품질 사례를 데이터베이스로 구축한 자체 개발 AI 플랫폼을 통해 과거 문서를 참조하여 표준작업절차서(Standard operating procedure)를 생성하고, 작업자가 신속하게 공정에 반영할 수 있도록 교육하고 있다”고 밝히며, AI 플랫폼과 함께 GMP 교육을 기반으로 한 삼성바이오로직스의 품질 교육 시간은 연간 21만 시간에 달한다고 전했습니다.
마침표 없는 세계
FDA는 지난 2022년, 의약품 부족의 60% 이상이 품질 이슈에서 발생한다고 언급하며, 단순한 규정 준수를 넘어 지속적인 의약품의 품질 개선을 이루고 강력한 품질 마인드 셋을 조성하기 위해 새로운 규제 관행으로 품질 관리 성숙도(QMM, Quality management maturity) 도입을 발표했습니다. ICH 또한 ICH Q10 모델*을 기반으로 전통적인 의약품 품질 개념에서 나아가 품질을 향하는 문화적 우수성과 운영 우수성을 포함하는 가이드라인을 제시하고 있습니다.
* 국제 의약품 규제 조화 위원회(ICH)가 개발한
의약품 산업을 위한 포괄적인 품질 관리 시스템 모델

품질 최우선 문화가 자연스럽게 스며들 수 있도록 삼성바이오로직스는 공정 중 일탈(deviation)이나 작업자의 오류(human error) 발생 시 자발적으로 공유하는 체계를 갖추고 있습니다. 품질 최우선 마인드와 견고한 시스템은 삼성바이오로직스가 글로벌 상위 제약사 20곳 중 17곳을 고객사로 확보할 수 있던 이유이기도 합니다.
정형석 팀장(Quality System&Compliance 팀)은 “삼성바이오로직스만의 품질 문화의 배경에는 함께 프로젝트를 수행하는 수많은 제약사들의 품질 시스템과 품질 마인드 셋을 경험하고 비교할 수 있는 글로벌 CDMO라는 특별한 위치가 있었다”고 설명하며, 품질은 우리 모두의 책임이고, 삼성바이오로직스의 존재 이유는 절대 타협할 수 없는 가치인 ‘품질’에 있다고 덧붙였습니다.
GMP 규정은 앞 글자에 대문자 C(Current)를 추가해 CGMP라는 이름으로도 불리는데, 이는 GMP규정이 고정 불변하는 것이 아니라 시대가 요구하는 수준에 맞게 적용되며 스스로 진화한다는 뜻을 내포합니다. 바이오의약품 품질의 세계에 마침표는 없기에, 삼성바이오로직스 역시 고품질의 바이오의약품을 환자에게 전달한다는 목표로 마침표 없는 품질을 향해 전진합니다.
Share article
Related Content