
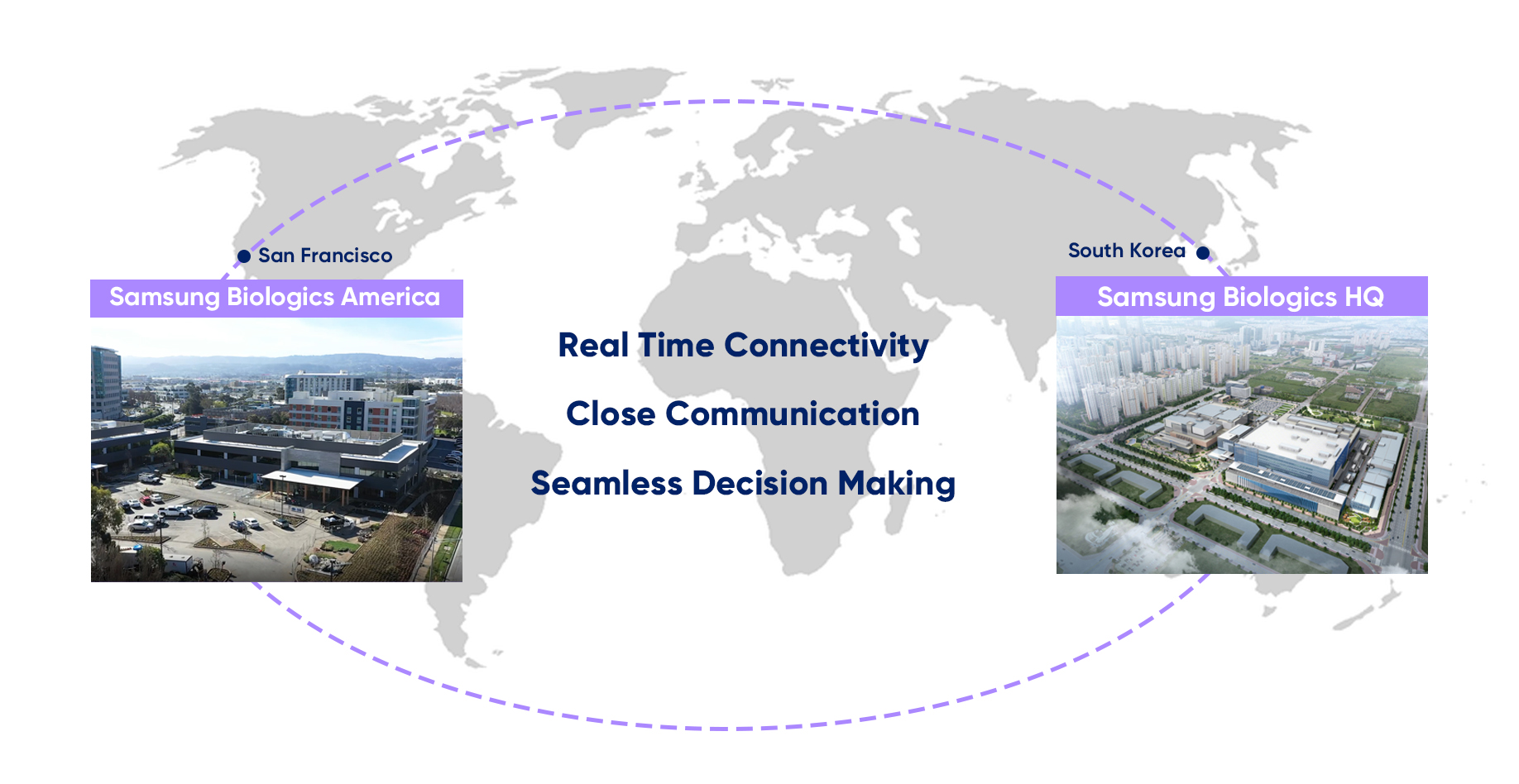
세계 최대 규모의 바이오의약품 생산기지인 삼성바이오로직스는 위탁생산(CMO)뿐 아니라 위탁개발(CDO)까지 사업 영역을 확장하며 원스톱 CDMO로서 글로벌 시장을 선점해 나가고 있는데요, 2020년 10월에는 미국의 대표 바이오 클러스터인 샌프란시스코에 R&D센터를 개소하며 고객사와의 물리적 거리를 좁히고, 신속한 서비스를 제공하는 ‘넥스트 도어(Next Door) CDO 파트너’가 되겠다고 밝혔습니다.
삼성바이오로직스의 차별화된 경쟁력 중 하나인 엔드 투 엔드 (End-to-End) 서비스, 그 첫 시작점인 바이오의약품 위탁개발과 삼성바이오로직스 위탁개발 서비스 경쟁력에 대해 소개해드립니다.
혁신 신약(First-in-Class)이 되기 위한 방법, 위탁개발(CDO)
신약 개발은 타깃 질병 후보물질을 발굴하는 ‘발견(Discovery)’ 단계와 전임상 및 임상시험을 실시해 신약 허가신청을 하는 ‘개발(Development)’ 단계로 구분됩니다. 위탁개발(CDO: Contract Development Organization)이란 신약개발 중 ‘개발’ 단계에 필요한 서비스(세포주 개발~임상 1상 물질 생산)를 제공하는 사업입니다.
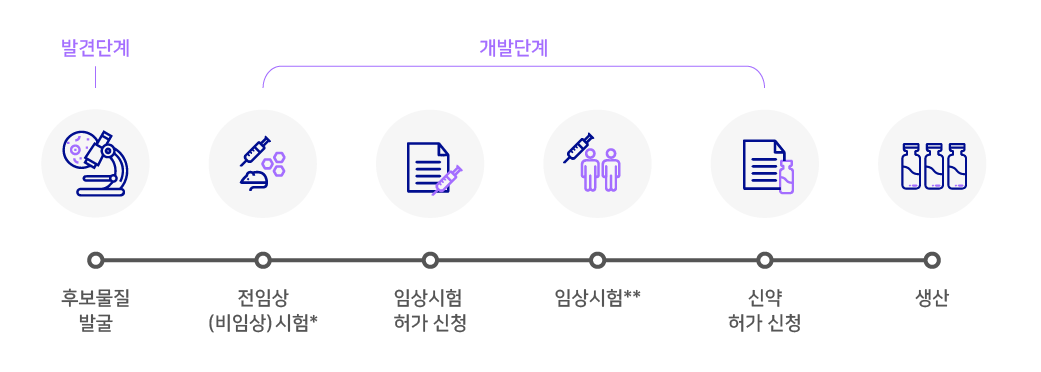
* 전임상(비임상) 시험: 동물 또는 세포를 대상으로 신약후보물질의 부작용이나 독성, 효과 등을 알아보는 시험
** 임상시험: 사람을 대상으로 신약후보물질의 안전성과 유효성을 증명하는 시험
신약 개발에는 막대한 자금과 기간이 소요되기에 특허를 취득한 바이오제약사는 출원 후 권리와 시장 독점권을 보장받습니다*나라별 기준 상이. 승자가 시장점유율에서 우위를 차지할 가능성이 큰 분야인 만큼 시간 싸움이 관건인데, ‘위탁개발’은 신약 개발 속도와 효율성을 높이기 위한 한 방법입니다.
바이오의약품 생산 시설이 없거나 부족한 버추얼 바이오테크나 소규모 바이오테크는 물론, 중소 제약사 등도 소규모 인력으로 연구개발(R&D)역량을 극대화하기 위해 대부분의 개발 활동을 위탁합니다. 생산 시설을 갖춘 글로벌 제약사도 특정 기술 도입이나 보완을 위해 일부 과정을 위탁해 개발하고 있습니다.
성공적인 신약 개발을 향한 여정
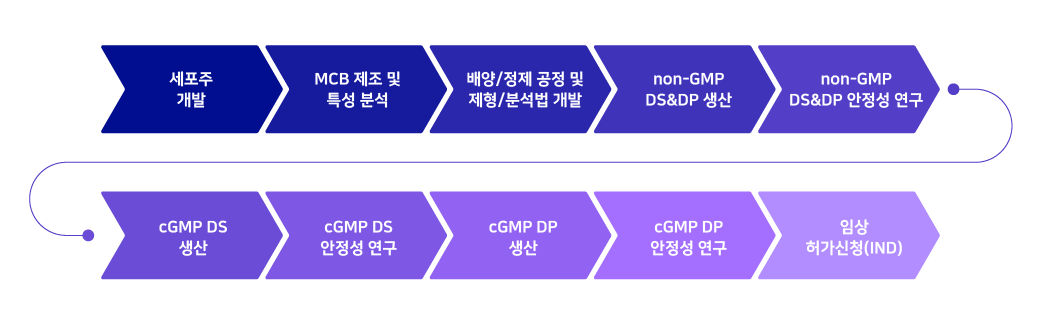
고객사가 초기 후보물질을 발굴해 위탁 개발을 의뢰하면 먼저 ‘세포주(Cell Line) 개발’에 착수합니다. 세포주란 목표 단백질을 생산할 수 있도록 유전자를 변형한 무한증식세포로, 생체 밖에서 대량 증식을 통해 항체의약품을 만들 수 있는 세포입니다.
고품질의 세포주 개발을 완료한 후에는 ‘공정, 제형 및 분석법 개발’을 진행하게 됩니다. 이후 전임상 시험에 필요한 ‘non-GMP 원료의약품(DS: Drug Substance)과 완제의약품(DP: Drug Product)’을 생산해 안정성 연구를 실시하고, ‘CGMP 원료의약품/완제의약품 생산 및 안정성 연구’를 마친 후에 ‘임상시험 허가 신청(IND: Investigational New Drug)’을 제출합니다.
삼성바이오로직스는 세포주 개발부터 공정·제형·분석법 개발, 임상시험계획(IND) 제출에 이르는 ‘개발 서비스’와 함께 비임상 및 글로벌 임상용 물질 ‘생산 서비스’ 등을 포함하는 통합 위탁개발 서비스를 제공합니다.
Faster and Better, 삼성바이오로직스 CDO 사업 경쟁력
삼성바이오로직스는 2020년 8월 자체 세포주 에스초이스(S-CHOice™)를 선보이며 고객의 선택 폭을 더 넓혔습니다. 에스초이스는 세포 분열 속도가 18~20시간으로 타사 세포주(만 하루, 24시간)보다 빠르게 번식합니다. 세포 발현량은 세포주 개발 직후 리터당 7그램 타이터(titer) 이상으로 업계 평균인 3~4그램 대비 두 배 가량 높고, 세포 생존율도 유가배양(fed-batch) 진행 시 21일까지 90% 이상으로 업계 평균(14일) 보다 높습니다. 따라서 에스초이스를 활용하면 대량 생산에 투입될 고품질 세포주를 보다 잘 선별할 수 있어 생산성을 향상시킬 수 있습니다.
세포주 개발 등의 과정을 거쳐 임상시험에 성공하면 세계 최대 규모의 바이오의약품 생산 기지인 송도 본사에 위탁생산(CMO)*을 의뢰할 수 있다는 점도 경쟁력입니다. 최고의 글로벌 전문가들이 제공하는 통합된 CDMO 서비스를 통해 의약품 안정성 및 품질을 유지하면서 차별화된 위탁생산을 경험할 수 있습니다.
(*위탁생산이 궁금하다면? '바이오의약품 위탁생산이 궁금해' 기사 읽으러 가기)
또한 샌프란시스코 R&D센터에 송도 본사의 최신 CDO 서비스 플랫폼을 그대로 구축해 고객사와의 지리적 접근성을 높였습니다. 삼성바이오로직스는 글로벌 확장을 통해 긴밀하고 신속한 커뮤니케이션으로 의약품 개발 과정을 지원하는 한편, 향후 보스턴, 유럽 등에도 R&D 센터를 추가로 구축해 고객사와의 물리적 거리를 좁히고 편의성을 높인다는 계획입니다.
From Gene to Commercialization, 신약 개발 파트너
위탁생산 서비스로 시작한 삼성바이오로직스는 급증하는 글로벌 위탁개발 수요에 대응하기 위해 포트폴리오를 확장, 글로벌 CDMO 업체로 단기간 내 빠르게 성장했습니다.
유연한 고객 맞춤형 서비스와 글로벌 품질 경쟁력을 바탕으로 신약 개발의 든든한 파트너로 자리매김한 삼성바이오로직스는 글로벌 트렌드에 맞춰 지속적으로 개발 역량을 강화해 고객 편의 제고를 위한 차별화된 서비스를 제공하고 있습니다.
삼성바이오로직스는 앞으로도 원스톱 서비스를 통해 더 빠르게 신약 개발을 지원하고, 바이오 생태계 선순환 구축에 노력하며, 전 세계의 더 많은 사람들이 질병에서 벗어날 수 있도록 하겠습니다.
관련 콘텐츠

세계 최대 규모의 바이오의약품 생산기지인 삼성바이오로직스는 위탁생산(CMO)뿐 아니라 위탁개발(CDO)까지 사업 영역을 확장하며 원스톱 CDMO로서 글로벌 시장을 선점해 나가고 있는데요, 2020년 10월에는 미국의 대표 바이오 클러스터인 샌프란시스코에 R&D센터를 개소하며 고객사와의 물리적 거리를 좁히고, 신속한 서비스를 제공하는 ‘넥스트 도어(Next Door) CDO 파트너’가 되겠다고 밝혔습니다.
삼성바이오로직스의 차별화된 경쟁력 중 하나인 엔드 투 엔드 (End-to-End) 서비스, 그 첫 시작점인 바이오의약품 위탁개발과 삼성바이오로직스 위탁개발 서비스 경쟁력에 대해 소개해드립니다.
혁신 신약(First-in-Class)이 되기 위한 방법, 위탁개발(CDO)
신약 개발은 타깃 질병 후보물질을 발굴하는 ‘발견(Discovery)’ 단계와 전임상 및 임상시험을 실시해 신약 허가신청을 하는 ‘개발(Development)’ 단계로 구분됩니다. 위탁개발(CDO: Contract Development Organization)이란 신약개발 중 ‘개발’ 단계에 필요한 서비스(세포주 개발~임상 1상 물질 생산)를 제공하는 사업입니다.

* 전임상(비임상) 시험: 동물 또는 세포를 대상으로 신약후보물질의 부작용이나 독성, 효과 등을 알아보는 시험
** 임상시험: 사람을 대상으로 신약후보물질의 안전성과 유효성을 증명하는 시험
신약 개발에는 막대한 자금과 기간이 소요되기에 특허를 취득한 바이오제약사는 출원 후 권리와 시장 독점권을 보장받습니다*나라별 기준 상이. 승자가 시장점유율에서 우위를 차지할 가능성이 큰 분야인 만큼 시간 싸움이 관건인데, ‘위탁개발’은 신약 개발 속도와 효율성을 높이기 위한 한 방법입니다.
바이오의약품 생산 시설이 없거나 부족한 버추얼 바이오테크나 소규모 바이오테크는 물론, 중소 제약사 등도 소규모 인력으로 연구개발(R&D)역량을 극대화하기 위해 대부분의 개발 활동을 위탁합니다. 생산 시설을 갖춘 글로벌 제약사도 특정 기술 도입이나 보완을 위해 일부 과정을 위탁해 개발하고 있습니다.
성공적인 신약 개발을 향한 여정

고객사가 초기 후보물질을 발굴해 위탁 개발을 의뢰하면 먼저 ‘세포주(Cell Line) 개발’에 착수합니다. 세포주란 목표 단백질을 생산할 수 있도록 유전자를 변형한 무한증식세포로, 생체 밖에서 대량 증식을 통해 항체의약품을 만들 수 있는 세포입니다.
고품질의 세포주 개발을 완료한 후에는 ‘공정, 제형 및 분석법 개발’을 진행하게 됩니다. 이후 전임상 시험에 필요한 ‘non-GMP 원료의약품(DS: Drug Substance)과 완제의약품(DP: Drug Product)’을 생산해 안정성 연구를 실시하고, ‘CGMP 원료의약품/완제의약품 생산 및 안정성 연구’를 마친 후에 ‘임상시험 허가 신청(IND: Investigational New Drug)’을 제출합니다.
삼성바이오로직스는 세포주 개발부터 공정·제형·분석법 개발, 임상시험계획(IND) 제출에 이르는 ‘개발 서비스’와 함께 비임상 및 글로벌 임상용 물질 ‘생산 서비스’ 등을 포함하는 통합 위탁개발 서비스를 제공합니다.
Faster and Better, 삼성바이오로직스 CDO 사업 경쟁력
삼성바이오로직스는 2020년 8월 자체 세포주 에스초이스(S-CHOice™)를 선보이며 고객의 선택 폭을 더 넓혔습니다. 에스초이스는 세포 분열 속도가 18~20시간으로 타사 세포주(만 하루, 24시간)보다 빠르게 번식합니다. 세포 발현량은 세포주 개발 직후 리터당 7그램 타이터(titer) 이상으로 업계 평균인 3~4그램 대비 두 배 가량 높고, 세포 생존율도 유가배양(fed-batch) 진행 시 21일까지 90% 이상으로 업계 평균(14일) 보다 높습니다. 따라서 에스초이스를 활용하면 대량 생산에 투입될 고품질 세포주를 보다 잘 선별할 수 있어 생산성을 향상시킬 수 있습니다.
세포주 개발 등의 과정을 거쳐 임상시험에 성공하면 세계 최대 규모의 바이오의약품 생산 기지인 송도 본사에 위탁생산(CMO)*을 의뢰할 수 있다는 점도 경쟁력입니다. 최고의 글로벌 전문가들이 제공하는 통합된 CDMO 서비스를 통해 의약품 안정성 및 품질을 유지하면서 차별화된 위탁생산을 경험할 수 있습니다.
(*위탁생산이 궁금하다면? '바이오의약품 위탁생산이 궁금해' 기사 읽으러 가기)
또한 샌프란시스코 R&D센터에 송도 본사의 최신 CDO 서비스 플랫폼을 그대로 구축해 고객사와의 지리적 접근성을 높였습니다. 삼성바이오로직스는 글로벌 확장을 통해 긴밀하고 신속한 커뮤니케이션으로 의약품 개발 과정을 지원하는 한편, 향후 보스턴, 유럽 등에도 R&D 센터를 추가로 구축해 고객사와의 물리적 거리를 좁히고 편의성을 높인다는 계획입니다.

From Gene to Commercialization, 신약 개발 파트너
위탁생산 서비스로 시작한 삼성바이오로직스는 급증하는 글로벌 위탁개발 수요에 대응하기 위해 포트폴리오를 확장, 글로벌 CDMO 업체로 단기간 내 빠르게 성장했습니다.
유연한 고객 맞춤형 서비스와 글로벌 품질 경쟁력을 바탕으로 신약 개발의 든든한 파트너로 자리매김한 삼성바이오로직스는 글로벌 트렌드에 맞춰 지속적으로 개발 역량을 강화해 고객 편의 제고를 위한 차별화된 서비스를 제공하고 있습니다.
삼성바이오로직스는 앞으로도 원스톱 서비스를 통해 더 빠르게 신약 개발을 지원하고, 바이오 생태계 선순환 구축에 노력하며, 전 세계의 더 많은 사람들이 질병에서 벗어날 수 있도록 하겠습니다.
관련 콘텐츠
Share article
Related Content